A medida que la edición genómica revoluciona la agricultura global, Chile se posiciona como un referente de América Latina con su marco regulatorio ágil, flexible y basado en la ciencia. Sin embargo, la falta de armonización internacional, los desafíos en la aceptación del mercado y la evolución de técnicas más complejas son puntos a considerar a la par del avance de estas innovaciones. ¿Cómo puede Chile consolidar su liderazgo y sortear estos obstáculos para impulsar la biotecnología agrícola? Averigualo en el siguiente reportaje sobre un reciente estudio publicado por nuestro Director Ejecutivo, Dr. Miguel Ángel Sánchez, en la revista científica Plants.
ChileBio / 27 de enero, 2025.- La edición genómica de plantas ha emergido como una herramienta revolucionaria en la agricultura moderna, permitiendo modificaciones precisas en los genomas de las plantas para mejorar su resistencia a plagas y enfermedades, tolerancia a factores climáticos, así como mayor productividad y calidad nutricional. Técnicas como CRISPR-Cas9 y TALENs han facilitado avances significativos en el fitomejoramiento, ofreciendo alternativas más rápidas y precisas que los métodos tradicionales. Sin embargo, la adopción y comercialización de estas tecnologías dependen en gran medida de los marcos regulatorios establecidos en cada país.
En un estudio publicado recientemente la revista Plants (Basel) por el Dr. Miguel Ángel Sánchez, Director Ejecutivo de ChileBio, se resalta como Chile destaca en este contexto por sido el segundo país del mundo (tras Argentina) en haber implementado en 2017 un marco regulatorio flexible y basado en la ciencia para las plantas desarrolladas mediante nuevas técnicas de mejoramiento (NBTs), que incluyen las técnicas de edición del genoma como CRISPR, TALEN, entre otras. Este enfoque ha posicionado al país como un líder en la promoción de la innovación agrícola y biotecnológica en América Latina.
Marco Regulatorio en Chile
El Servicio Agrícola y Ganadero (SAG), dependiente del Ministerio de Agricultura, es la entidad encargada de regular la biotecnología agrícola en Chile. Aunque el país no ha ratificado el Protocolo de Cartagena, utiliza su definición de organismo genéticamente modificado (OGM) para abordar las NBTs, considerando como OGM a cualquier organismo vivo con una combinación novedosa de material genético obtenida mediante biotecnología moderna. Sin embargo, Chile ha clarificado este concepto, definiendo una combinación novedosa como la inserción estable de uno o más genes o secuencias de ADN que codifican proteínas, ARN de interferencia, ARN de doble hebra, péptidos señal o secuencias regulatorias introducidas permanentemente en el genoma de la planta. De esta manera, los productos desarrollados mediante NBTs que no contienen ADN exógeno en el producto final no se consideran OGMs (transgénicos) y se tratan como convencionales.
El Dr. Sánchez destava que «el proceso regulatorio en Chile no es una autorización, sino una determinación caso por caso para establecer si un producto vegetal es un OGM o no«. El formulario de solicitud consta de dos secciones: información del solicitante e información técnica sobre la taxonomía, cultivares o líneas, fenotipo, técnica biotecnológica utilizada, determinación de la ausencia de ADN foráneo e indicación de si el material de propagación ha sido autorizado por alguna agencia oficial en otro país. «El tiempo de respuesta es de 20 días hábiles, y el proceso ha sido elogiado por su simplicidad, rapidez y predictibilidad», describe el investigador.
[Recomendado: Investigadores chilenos desarrollan poroto tolerante a la sequía mediante edición del genoma]
Productos editados que han pasado por el sistema chileno
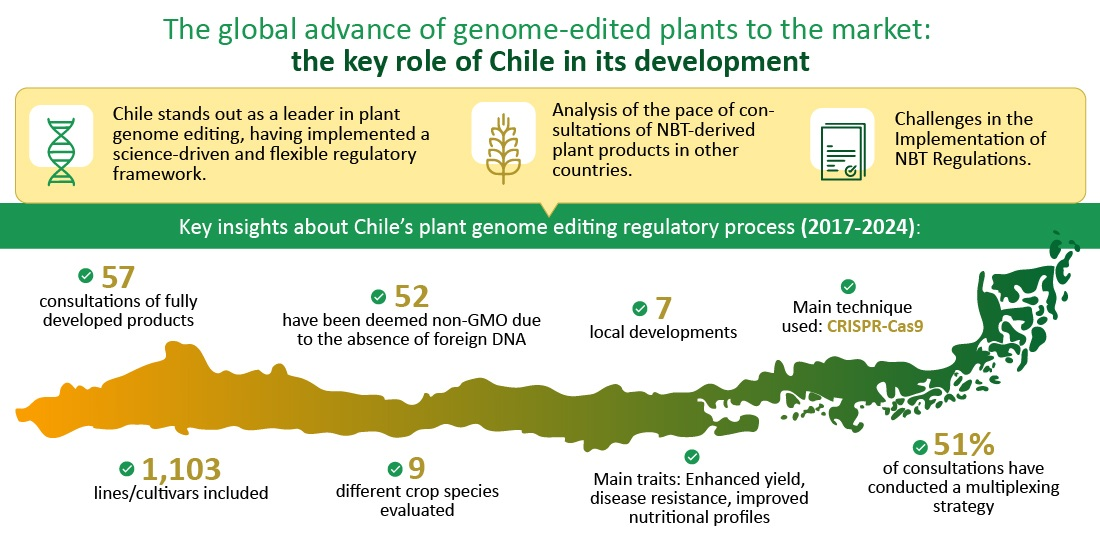
Desde la implementación del marco regulatorio en 2017 hasta noviembre de 2024, el estudio indica que el SAG ha recibido 57 solicitudes, de las cuales 52 fueron consideradas no OGMs debido a la ausencia de material genético foráneo, y 5 fueron clasificadas como OGMs. Estas últimas incluyeron casos donde, aunque se utilizó cisgénesis, se empleó un promotor de una especie no sexualmente compatible, o donde el sistema CRISPR/Cas aún estaba insertado en el genoma de la planta. Estas evaluaciones destacan la capacidad del marco chileno para analizar productos editados genéticamente caso por caso, asegurando decisiones basadas en las características específicas de cada aplicación.
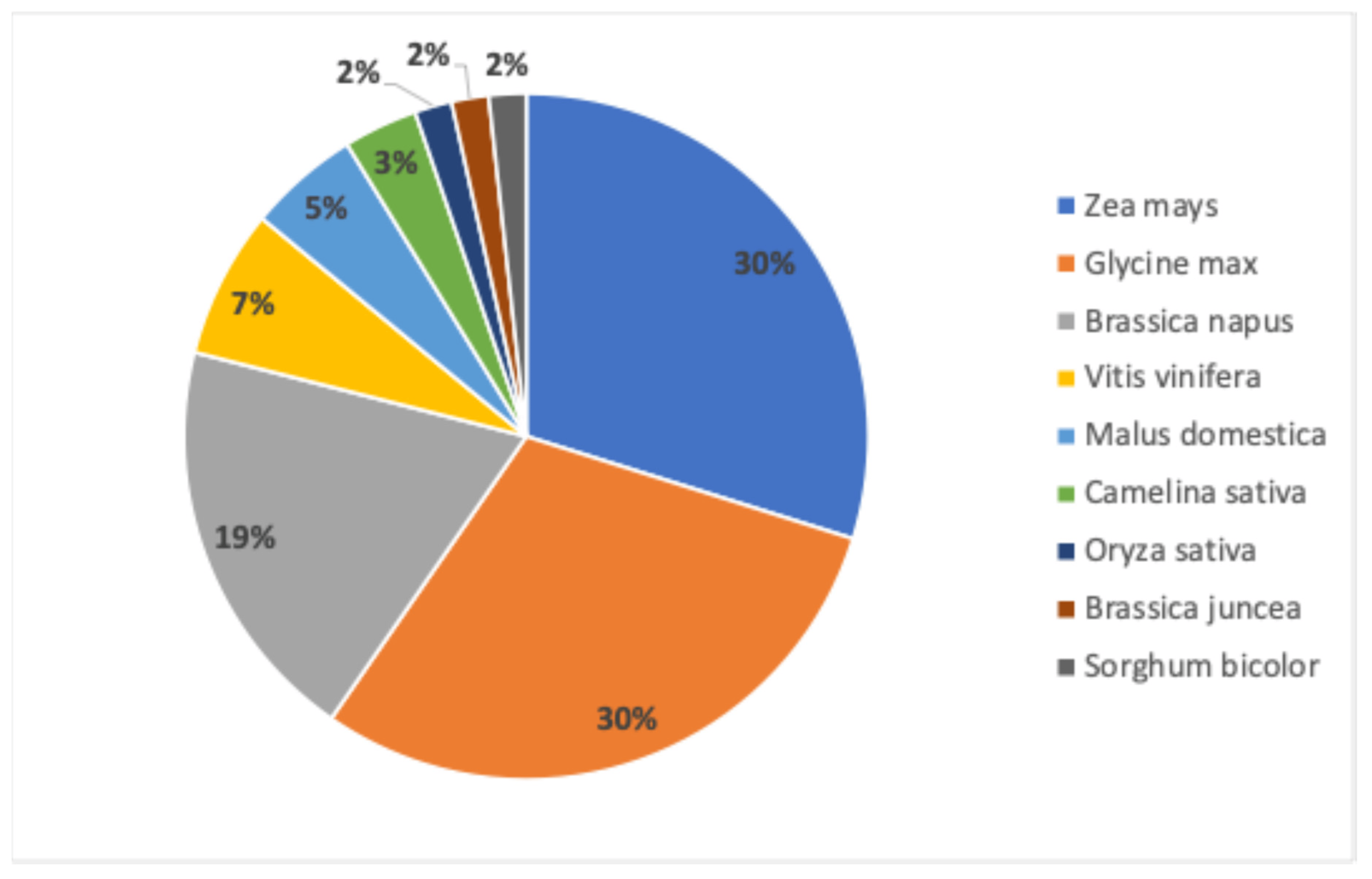
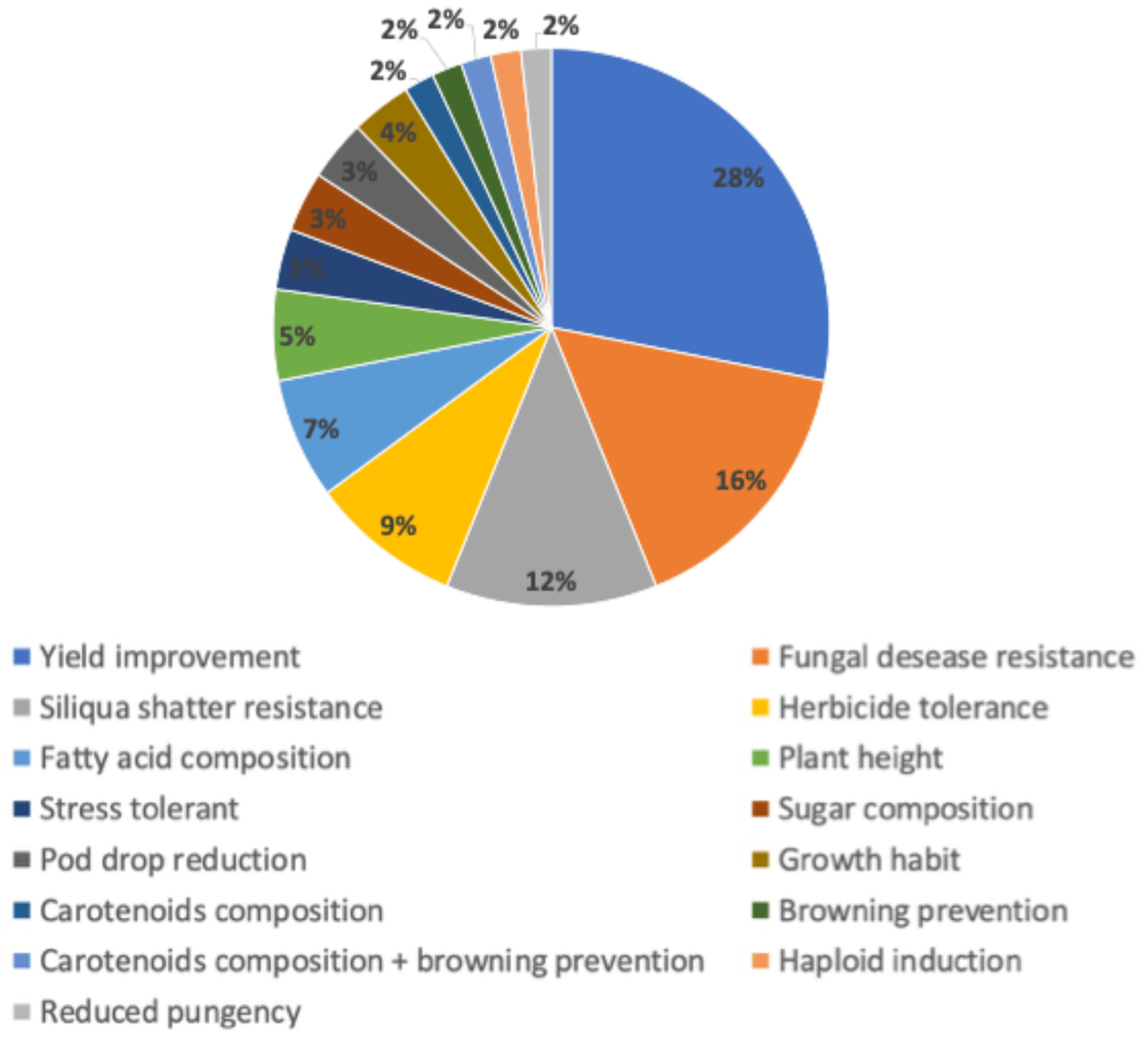
Las solicitudes han abarcado nueve especies de cultivos diferentes, siendo el maíz y la soja las más comunes. Las características fenotípicas más buscadas incluyen mejoras en el rendimiento, resistencia a enfermedades fúngicas y resistencia al desgrane de vainas. La técnica CRISPR-Cas9 es la más utilizada, reflejando tendencias globales en preferencias de edición genómica.
[Recomendado: La apuesta científica de forestal chilena en EEUU: adquiere startup biotech enfocada en edición genética]
Chile ha atraído solicitudes tanto de desarrolladores locales como extranjeros, con 7 de las 57 aplicaciones provenientes de instituciones locales y 50 de entidades extranjeras, lo que refleja un interés internacional en utilizar la vía regulatoria chilena.
El Dr. Sanchez destaca que «de las 57 solicitudes ya presentadas al sistema regulatorio chileno, estas incluyeron no 57 sino 1103 líneas. Solo 21 solicitudes (37%) incluyen solo una línea/cultivar para ser evaluado por el SAG. Curiosamente, 16 solicitudes contienen más de 10 líneas, 6 tienen más de 50 y 4 tienen más de 100«. Agrega que «la solicitud que incluyó la mayor cantidad de líneas fue una con 270″.
Por otro lado, el investigador describe que las solicitudes presentadas indican una tendencia hacia la multiplexación, donde se editan varios genes simultáneamente para crear fenotipos complejos o se edita un solo gen en diferentes regiones. Esta capacidad es cada vez más importante para desarrollar rasgos multifacéticos, como la resistencia a rasgos climáticos y el aumento del rendimiento. En el caso del marco regulatorio de NBT de Chile, el 51% de las 57 solicitudes presentadas han incluido una estrategia de multiplexación.
Además, el enfoque regulatorio permite la presentación de múltiples líneas obtenidas de un solo proceso de edición genómica bajo una única solicitud, lo que agiliza el proceso de evaluación y reduce las cargas administrativas.
[Recomendado: INIA y Biofrutales logran importante avance científico en edición genética frutal en Chile]
Panorama Internacional de la Regulación de cultivos editados genéticamente
A nivel global, la adopción de NBTs en plantas avanza, impulsada por su potencial para abordar desafíos relacionados con la seguridad alimentaria, la sostenibilidad y la resiliencia climática. Sin embargo, los marcos regulatorios varían significativamente entre regiones, influyendo en la velocidad y alcance de la adopción tecnológica.
Por ejemplo, Estados Unidos ha adoptado un enfoque basado en el producto, centrándose en las características del producto final en lugar del proceso utilizado para crearlo. El Departamento de Agricultura de EE. UU. (USDA) exime de la regulación de OGMs aquellas modificaciones que podrían lograrse mediante mejoramiento convencional. Hasta noviembre de 2024, se han presentado 99 solicitudes de confirmación desde 2021, y cuatro plantas editadas genéticamente han sido introducidas en el mercado estadounidense: SU Canola™, una canola tolerante a herbicidas desarrollada mediante mutagénesis dirigida por oligonucleótidos; una soja productora de aceite Calyno™, creada con tecnología TALEN, con un alto contenido de ácido oleico, grasas saturadas reducidas y sin grasas trans; la ensalada Conscious™, hojas de mostaza editadas con CRISPR para reducir el picante y mejorar su sabor; y una lechuga romana GreenVenus™, una variedad que no se pardea al cortarla y se mantiene fresca y crujiente hasta dos semanas en comparación a las lechugas convencionales.
[Recomendado: CRISPR y la nueva era del fitomejoramiento de precisión: conversación con el Dr. Tom Adams, Director Ejecutivo de Pairwise]
Canadá, por su parte, cuenta con un marco regulatorio basado en la novedad, evaluando los rasgos novedosos independientemente del proceso de desarrollo. Los desarrolladores pueden auto-determinar la novedad de sus rasgos y, si una planta editada genéticamente no exhibe un rasgo novedoso, está exenta de una mayor evaluación regulatoria. Hasta octubre de 2024, hay una lista de 14 productos no novedosos de mejoramiento vegetal destinados al uso alimentario en Canadá.
Brasil, Colombia y Argentina también han establecido procesos de consulta caso por caso para determinar si un producto obtenido por NBTs debe ser clasificado como OGM.
«Argentina fue el primer país a nivel mundial en abordar el tema al regular los productos derivados de NBT en 2015, y sus reguladores han contribuido activamente a los avances técnicos y regulatorios para NBT en América del Sur, África y Asia» afirma el Sanchez. En el ámbito de la Comisión Nacional Asesora de Biotecnología Agropecuaria (CONABIA), se ha establecido un enfoque basado en productos para analizar si se genera una nueva combinación de material genético en plantas, animales y microorganismos.
Las consultas a analizar por CONABIA pueden incluir productos completamente desarrollados o desarrollos en etapas tempranas. En esta última situación, el solicitante debe presentar posteriormente un segundo formulario cuando el producto esté terminado para verificar si los cambios genéticos introducidos coinciden con los descriptos en la primera consulta. CONABIA tiene 80 días hábiles para dar una respuesta oficial, concluyendo si el producto es OGM o convencional. Desde 2015, CONABIA ha recibido 92 consultas relacionadas con plantas derivadas de NBT completamente desarrolladas y 32 consultas para plantas en etapa temprana de desarrollo (hasta noviembre de 2024).
En el caso de Brasil, a noviembre de 2024, y desde 2018, la CTNBio ha concluido que 16 consultas sobre productos vegetales derivados de NBT no califican como OGMs.
En Asia, Japón y Filipinas han implementado directrices que clasifican las plantas editadas genéticamente de manera diferente a los OGMs, siempre que no contengan ADN foráneo.
En el caso de Japón, en 2019 estableció un marco regulatorio en el que las plantas editadas genéticamente no se consideran OGMs siempre que no contengan ADN foráneo en su genoma final. Este enfoque permite que las plantas desarrolladas mediante edición genética sean tratadas de manera similar a las variedades convencionales, lo que facilita su comercialización sin la necesidad de largos procesos regulatorios. Japón ha sido uno de los primeros países en aprobar y comercializar alimentos editados genéticamente, como el tomate GABA, que posee altos niveles de ácido gamma-aminobutírico, un compuesto con beneficios para la salud.
Filipinas ha adoptado un enfoque similar al de Japón, diferenciando las plantas editadas genéticamente de los OGMs tradicionales. La Autoridad Nacional de Biotecnología (DA-Biotech) establece que si la edición genética no implica la inserción de ADN foráneo, el producto se considera equivalente a una variedad convencional. Este marco regulatorio ha permitido el desarrollo de variedades de arroz y berenjena editadas genéticamente con resistencia a enfermedades y mayor rendimiento.
[Recomendado: Filipinas aprueba producción comercial de plátano y tomate editado genéticamente con beneficios nutricionales y ambientales]
A diferencia de Japón y Filipinas, China ha adoptado un enfoque más cauteloso. En 2022, el Ministerio de Agricultura y Asuntos Rurales (MARA) introdujo directrices que distinguen los cultivos editados genéticamente de los OGMs (transgénicos) si no implican la introducción de ADN extraño. Sin embargo, bajo este marco, los productos editados genéticamente caen dentro del alcance de las regulaciones de OGM y están regulados como OGM. Los productos vegetales derivados de NBT deben obtener un certificado de seguridad después de las pruebas de campo, las evaluaciones de seguridad y la aprobación final del MARA. Con base en un análisis caso por caso, los cultivos editados genéticamente sin ADN extraño se clasifican en cuatro categorías con respecto al perfil de riesgo del rasgo de interés. En lugar de los casi 10 años requeridos para los certificados de seguridad de OGM, los productos vegetales derivados de NBT pueden obtener un certificado de seguridad en 1 o 2 años, afirma el estudio.
[Recomendado: China aprueba más cultivos transgénicos y editados para aumentar los rendimientos y garantizar la seguridad alimentaria]
A partir de noviembre de 2024, MARA ha emitido cinco certificados de seguridad para productos vegetales derivados de NBTs, incluidos soja (3), maíz (1) y trigo (1).
Desafíos en los sistemas regulatorios a nivel internacional
El estudio indica que Chile ha demostrado un enfoque regulatorio ágil y basado en la ciencia que ha fomentado la innovación en la biotecnología agrícola. Sin embargo, existen desafíos que deben abordarse para consolidar al país como un líder en la adopción de NBTs:
- Barreras precomerciales y regulatorias: Los desarrolladores enfrentan incertidumbre sobre los requisitos regulatorios en etapas tempranas, lo que genera ineficiencias y pérdida de recursos. Modelos como el de Argentina, que permite consultas regulatorias en fase temprana de un cultivo en desarrollo, podrían mejorar este aspecto. Además, la falta de armonización en los requisitos de datos obliga a cumplir múltiples estándares, encareciendo costos y retrasando la comercialización.
- Requisitos postcomerciales innecesarios: Dado que los productos derivados de NBTs son indistinguibles de variedades convencionales, exigencias como etiquetado y trazabilidad no tienen justificación técnica. Sin embargo, algunos marcos regulatorios aún imponen estas medidas, generando costos adicionales y barreras de mercado.
- Diferencias regulatorias y barreras al comercio internacional: La variabilidad entre regulaciones nacionales crea incertidumbre y afecta la exportación de cultivos editados genéticamente. Chile, con su sistema eficiente, enfrenta dificultades para acceder a mercados como los asiáticos, donde los requisitos son más restrictivos. Sin acuerdos globales, los desarrolladores deben sortear obstáculos que encarecen y limitan la comercialización.
- Falta de adaptación a modificaciones genéticas complejas: Las regulaciones actuales se centran en la presencia o ausencia de ADN foráneo, pero nuevas técnicas permiten modificaciones más avanzadas, como translocaciones y cambios en el número de copias génicas. Estas no están contempladas en los marcos regulatorios, lo que podría generar retrasos y discrepancias entre países, afectando la adopción y el comercio de estos productos.
- Percepción pública y aceptación del mercado: Más allá de las regulaciones, la aceptación social de los cultivos editados genéticamente es crucial. La confusión con los transgénicos, el escepticismo sobre su seguridad y el desconocimiento de sus beneficios pueden generar resistencia en consumidores y productores afirma el estudio. Además, la dependencia de mercados internacionales impone desafíos adicionales, ya que algunas regiones podrían rechazar estos productos independientemente de su estatus regulatorio.
El marco regulatorio de Chile basado en productos lo posiciona entre los regímenes regulatorios más favorables a la innovación, atrayendo a desarrolladores internacionales con sus procesos claros y simplificados para productos clasificados como no transgénicos, posicionando al país como un referente en América Latina.
«Este sistema, basado en la presencia o ausencia de ADN extraño (un criterio global ampliamente aceptado y el estándar principal para distinguir las plantas editadas genómicamente de las transgénicas), brinda funcionalidad, flexibilidad y previsibilidad«.
«El modelo regulatorio de Chile se destaca por dar cabida a innovaciones como la multiplexación y el desarrollo de múltiples líneas por proceso de edición, lo que alienta a los fitomejoradores a realizar pruebas de campo y multiplicar localmente las semillas en contraestación» afirma el Dr. Sánchez.
«Chile debe adaptar proactivamente su marco para mantener su liderazgo, equilibrando la innovación con la seguridad y las demandas del mercado. El fortalecimiento de la colaboración con los organismos regulatorios y científicos globales ayudará a alinear las prácticas con los estándares internacionales, manteniendo al mismo tiempo la flexibilidad para los nuevos productos de NBT. La transparencia y la participación pública respecto de los beneficios y la seguridad de la edición del genoma serán vitales para fomentar la aceptación y maximizar el impacto de las NBT en la agricultura sostenible» concluye el Dr. Sánchez.

